Конспект урока + презентация по теме "Химические свойства металлов" (9 класс, учебник О.С. Габриеляна)
Образовательный портал «Мой университет» - www.moi-universitet.ru
Факультет «Реформа образования» - www.edu-reforma.ru
Подробный конспект урока.
|
Организационная информация |
|||||||||||||||||||||||||||
|
Тема урока
|
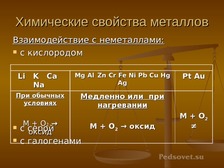
Химические свойства металлов |
||||||||||||||||||||||||||
|
Предмет |
Химия |
||||||||||||||||||||||||||
|
Класс |
9 |
||||||||||||||||||||||||||
|
Автор урока (ФИО, должность) |
Зайберт Инна Сергеевна, учитель химии |
||||||||||||||||||||||||||
|
Образовательное учреждение |
Муниципальное образовательное учреждение Светлолобовская средняя общеобразовательная школа №6 имени героя России Мудрова М.И. |
||||||||||||||||||||||||||
|
Методическая информация |
|||||||||||||||||||||||||||
|
Тип урока
|
Изучение нового |
||||||||||||||||||||||||||
|
Цели урока
|
Образовательные – создать условия для изучения химических свойств металлов Развивающие – развивать познавательную активность учащихся, способствовать развитию умений наблюдать, делать выводы на основе результатов своих исследований Воспитательные – воспитание положительной мотивации учения. |
||||||||||||||||||||||||||
|
Задачи урока
|
|
||||||||||||||||||||||||||
|
Знания, умения, навыки и качества, которые актуализируют/приобретут/закрепят/др. ученики в ходе урока |
Формирование знаний о химических свойствах металлов, умения наблюдать, делать выводы на основе результатов своих исследований |
||||||||||||||||||||||||||
|
Необходимое оборудование и материалы |
Компьютер, проектор, реактивы: раствор соляной кислоты, натрий, цинк, медь, железо, сульфат меди, вода, фенолфталеин.
|
||||||||||||||||||||||||||
|
Подробный конспект урока |
|||||||||||||||||||||||||||
|
Мотивация учащихся
|
|
||||||||||||||||||||||||||
|
Ход и содержание урока
|
|
||||||||||||||||||||||||||
|
Проверка и оценивание ЗУНКов
|
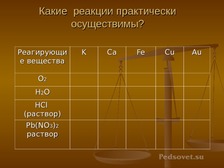
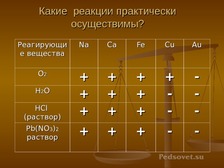
А теперь на основании ваших знаний заполните таблицу. |
Заполняют таблицу. Самопроверка. |
|||||||||||||||||||||||||
|
Итог урока |
В течение всего урока мы изучали химические свойства металлов, делали выводы, подтвердили гипотезы. Вы почти убедили меня, но все-таки я хочу еще раз проверить. (опыт: золотое кольцо с соляной кислотой)
|
Да, гипотезы оказались верны |
|||||||||||||||||||||||||
|
Рефлексия деятельности на уроке
|
Я приготовила для вас небольшой сюрприз. Посмотрите на экран и улыбнитесь вместе со мной. |
||||||||||||||||||||||||||
|
Домашнее задание
|
Дополнить таблицу уравнениями реакций. |
||||||||||||||||||||||||||
|
В помощь учителю |
|||||||||||||||||||||||||||
|
Использованные источники и литература (если имеются) |
Учебник для общеобразовательных учреждений / О.С. Габриелян, «Дрофа»
|
||||||||||||||||||||||||||
На странице приведен фрагмент.
|
Автор: Зайберт Инна Сергеевна
→ Инна5587 |
Спасибо за Вашу оценку. Если хотите, чтобы Ваше имя
стало известно автору, войдите на сайт как пользователь
и нажмите Спасибо еще раз. Ваше имя появится на этой стрнице.